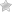Трофобластическая болезнь – общее понятие, объединяющее различные формы ассоциированной с беременностью пролиферативной неоплазии трофобласта. Термин «трофобластическая болезнь» включает в себя пузырный занос (частичный и полный), инвазивный пузырный занос, хорионкарциному, эпителиоидную трофобластическую опухоль, трофобластическую опухоль плацентарной площадки. Диагностика трофобластической болезни основывается на данных УЗИ и КТ, исследования концентрации ХГЧ в крови. Лечение может включать эвакуацию пузырного заноса, химиотерапию, гистеротомию.
В гинекологии трофобластическая болезнь является довольно редкой патологией и встречается в 1—2,5% случаев; ее развитие ассоциировано с беременностью; первичной локализацией практически всегда служит матка.
Среди различных форм трофобластической болезни на полный пузырный занос приходится 72,2% случаев; на частичный – 5%; на хорионкарциному — 17,5%, другие виды — 5,3%. При трофобластической болезни возникают пролиферативные аномалии наружного слоя клеток зародыша, участвующих в формировании эпителиального покрова ворсин хориона.
Возникновение трофобластической болезни возможно как во время гестации, так и после завершения беременности. Трофобластическая болезнь может иметь доброкачественное или злокачественное течение.
Трофобластическая болезнь
Международная классификация различает доброкачественные формы трофобластической болезни (частичный и полный пузырный занос) и злокачественные неоплазии (инвазивный пузырный занос, хорионкарциному, трофобластическую опухоль плацентарного ложа, эпителиоидноклеточную трофобластическую опухоль). Злокачественные неоплазии могут иметь неметастазирующее и метастазирующее клиническое течение низкой либо высокой степени риска.
Согласно клинической классификации FIGO, выделяют следующие стадии трофобластической болезни:
- I – локализация трофобластического новообразования ограничена маткой
- II – трофобластическая неоплазия распространяется на широкую связку матки, придатки, влагалище, но ограничивается гениталиями.
- III – кроме поражения половых органов, определяются метастазы в легкие
- IV – кроме легочных метастазов, определяются поражения селезенки, почек, ЖКТ, печени, головного мозга.
Различные формы трофобластической болезни рассматриваются онкогинекологией как единый этиопатогенетический процесс. Среди этиологических предпосылок трофобластической болезни не исключаются особые свойства яйцеклетки, влияние вирусов (в частности, вируса гриппа) на трофобласт, иммунологические факторы, повышение активности гиалуронидазы, хромосомные аберрации, дефицит белка.
Замечено, что вероятность развития трофобластической болезни в 5 раз выше у женщин старше 40 лет, чем у женщин до 35 лет.
Среди других факторов риска выделяют наличие в анамнезе эпизодов самопроизвольного прерывания беременности, абортов, внематочной беременности, родов.
В географическом плане трофобластическая болезнь чаще развивается у жительниц Востока, чем у представительниц западных стран.
Шансы на развитие хорионкарциномы значительно возрастают после перенесенного пузырного заноса по сравнению с нормально протекающей беременностью.
В свою очередь, вероятность развития инвазивного пузырного заноса выше после полной формы пузырного заноса, чем после частичной.
Трансформация структур трофобласта может развиваться в процессе беременности (нормальной или эктопированной) либо после завершения гестации (родов, выкидыша, аборта).
Клиника пузырного заноса характеризуется влагалищными кровотечениями (90%); превышением размеров матки должной величины, соответствующей сроку гестации (50%); двусторонними текалютеиновыми кистами более 8 см в диаметре (до 40% случаев).
Течение пузырного заноса может осложняться токсикозом беременных (неукротимой рвотой), артериальной гипертензией, преэклампсией, признаками гипертиреоза (гипертермией, тахикардией и др.), разрывом овариальных кист, профузным кровотечением.
В редких случаях при данной форме трофобластической болезни развивается ТЭЛА, ДВС-синдром.
Клиническими особенностями инвазивного пузырного заноса служит инфильтративный рост, высокая вероятность трансформации в хорионкарциному, в трети случаев — метастазирование в вульву, влагалище, легкие.
Трофобластическая хорионкарцинома способна глубоко инфильтрировать и разрушать стенку матки, поэтому обычно первым проявлением данной формы трофобластической болезни служит массивное кровотечение.
Хорионкарцинома обладает высокой частотой метастазирования в легкие, органы малого таза, печень, селезенку, головной мозг, почки, желудок, обуславливая соответствующую клиническую симптоматику.
Трофобластическая опухоль плацентарного ложа обладает инфильтрирующим ростом, что сопровождается разрушением серозного покрова матки, кровотечениями; может метастазировать во влагалище, брюшную полость, головной мозг.
Эпителиоидноклеточная трофобластическая опухоль чаще имеет локализацию в области дна матки и в цервикальном канале, что может проявляться признаками, типичными для рака тела или шейки матки.
Данная форма трофобластической болезни нередко манифестирует спустя несколько лет после беременности, заявляя о себе наличием отдаленных метастазов.
В связи с наличием метастазов могут отмечаться головные боли, боли в грудной клетке, кашель с выделением кровянистой мокроты, желудочные кровотечения, кишечная непроходимость, парезы, интоксикация, анемия, кахексия и т. д. При различных формах трофобластической болезни могут возникать боли в животе, связанные с прорастанием опухолью параметрия, сдавлением нервных стволов, перфорацией матки, разрывом или перекрутом ножки кисты.
В анамнезе у всех пациенток с трофобластической болезнью отмечается беременность, завершившаяся абортами (искусственными или самопроизвольными), родами, тубэктомией по поводу внематочной беременности.
Большинство пациенток жалуется на аменорею, ациклические маточные кровотечения, олигоменорею, меноррагии, боли в животе или груди, головную боль, кровохарканье, кашель.
Во время гинекологического исследования обнаруживаются увеличенные размеры матки, не соответствующие должному сроку беременности или послеродового периода. Нередко гинекологу удается пропальпировать опухолевые узлы в матке, малом тазу, влагалище.
Использование трансвагинального УЗИ позволяет обнаружить опухоли трофобласта с минимальным размером 4 мм. Патогномоничным признаком трофобластической болезни является обнаружение текалютеиновых кист яичников, часто больших размеров.
Концентрация ХГЧ в плазме крови при трофобластической болезни всегда повышена.
Важнейшим критерием диагностики трофобластической болезни служит морфологическое исследование тканей, полученных в ходе диагностического выскабливания матки, лапароскопии, иссечения опухолей стенки влагалища, пункции метастазов.
С помощью вспомогательных методов (УЗИ брюшной полости, печени, почек; КТ, ПЭТ, МРТ головного мозга; рентгенографии грудной клетки, КТ легких; тазовой ангиографии) определяются метастазы в малом тазу и отдаленных органах. При выявлении метастазов экстрагенитальной локализации возникает необходимость в консультации абдоминального хирурга, пульмонолога, нейрохирурга, уролога и т. д.
Лечебная тактика при трофобластической болезни определяется ее формой и стадией. При пузырном заносе производится его вакуум-экстракция с контрольным кюретажем полости матки. Обязательно назначение контрацепции в течение года после удаления пузырного заноса.
Химиотерапия при динамическом снижении ХГЧ не назначается.
Во всех случаях трофобластической болезни со злокачественным течением показано проведение химиотерапии по одной из схем (метотрексат + дактиномицин; этопозид + цисплатин; дактиномицин + метотрексат + цисплатин + винкристин).
Хирургическая тактика обоснована при угрожающем кровотечении из первичной опухоли, перфорации стенки матки, резистентности к химиотерапии. У больных репродуктивного возраста возможно выполнение органосохраняющей гистеротомии с иссечением опухолевых тканей; у пациенток, не планирующих деторождение, целесообразно удаление матки методом надвлагалищной ампутации или радикальной гистерэктомии.
После курса терапии осуществляется мониторинг ХГЧ и характера менструального цикла, эхографический контроль, динамическая рентгенография легких, по показаниям – МРТ головного мозга в течение 2-3-х лет. Беременность женщинам, перенесшим трофобластическую болезнь, разрешается, не ранее, чем через 12-18 мес. после излечения.
Правильность и своевременность лечения трофобластической болезни гарантирует в абсолютном большинстве случаев хороший прогноз. Химиотерапия позволяет вылечить 100% пациенток с неметастазирующим течением трофобластической болезни и около 70% с метастазирующими формами.
У молодых женщин обычно удается сохранить генеративную функцию. Дальнейшее наблюдение и обследование, ведение менограммы и контрацепция позволяют рассчитывать на успешное протекание последующей беременности. Рецидивы трофобластической болезни наблюдаются в 3-8% случаях.
Morphological changes in the fallopian tubes in patients with ectopic pregnancy | Titova | Gynecology
Relevance. Ectopic pregnancy is an urgent condition which may lead to intraabdominal hemorrhage and woman death. In recent years, the frequency of this pathology is significantly increasing. However, morphological changes in the fallopian tubes in patients with this disease remain understudied.
Aim. To study morphological changes in the fallopian tubes in patients with ectopic pregnancy with various variants of the clinical course.
Materials and methods. The morphological study included 130 patients who had laparoscopic surgery for ectopic pregnancy. Comprehensive morphological study of the fallopian tubes removed during surgery was conducted.
Results and discussion. The article presents the morphological changes in the fallopian tubes in patients with ectopic pregnancy.
Implantation of a fertilized egg in the fallopian tube led to significant changes in its macro- and microstructure, which were due to invasion of the chorionic villi and involved all layers of the tube wall, differing only in depth and prevalence.
The most pronounced morphological changes in various segments of the tube were revealed in the endosalpinx.
Conclusion. The combination of morphological changes in different layers of the tube is related to a chronic non-specific productive endomyosalpingitis with luminal deformation, which was one of the main causes of this disease development.
ectopic pregnancy, laparoscopy, morphological study .
Внематочная (эктопическая) беременность – одно из наиболее грозных гинекологических заболеваний, требующих оказания неотложной медицинской помощи [1–3]. Трубная локализация является наиболее частой формой этой патологии [4–7].
Внематочная беременность относится к ургентным состояниям, связанным с возможностью развития внутрибрюшного кровотечения и летального исхода для женщины [3, 8, 9].
Внематочная беременность занимает одно из ведущих мест в структуре материнской смертности, стоит на первом месте как причина внутрибрюшного кровотечения и на втором месте в структуре острых гинекологических заболеваний [5, 10–12]. Пациентки с данной патологией составляют 2–12,6% от общего числа женщин, госпитализируемых в гинекологические стационары [2, 10].
Частота внематочной беременности не имеет тенденции к снижению и в настоящее время в 2 раза превышает показатель 30-летней давности [2, 4, 6, 12]. Так, если в середине ХХ в. частота данной патологии составляла 4,2–9,9 больных на 1 тыс. беременных женщин, то в последние годы она возросла до 18,8 случаев на 1 тыс. беременностей [5, 6, 9, 13–15].
Самым достоверным методом диагностики трубной беременности является морфологическое исследование удаленного органа при его гистологическом исследовании [16–18].
Однако до настоящего времени остаются малоизученными морфологические изменения маточных труб у больных с трубной беременностью.
Анализ этих результатов может позволить клиницистам разрабатывать дифференцированный подход к оптимальным методикам лечения у больных с разными вариантами клинического течения данной патологии.
Цель настоящего исследования – изучение морфологических изменений в маточных трубах при разных вариантах клинического течения у больных с трубной беременностью.
Материалы и методы
Морфологическое исследование выполнено у 130 больных, перенесших оперативное лечение по поводу трубной беременности с использованием лапароскопического метода. Проведено детальное морфологическое исследование всех маточных труб, удаленных во время операции.
При выполнении лапароскопии была диагностирована локализация плодовместилища в разных отделах маточной трубы (см. таблицу).
| Локализация трубной беременностиTubal pregnancy localization | ||
| Отдел трубы | Число больных | % |
| Ампулярный | 108 | 83,1 |
| Истмический | 19 | 14,6 |
| Интерстициальный | 3 | 2,3 |
| Всего | 130 | 100 |
Отмечено, что в большинстве случаев (108 – 83,1%) плодное яйцо располагалось в ампулярном отделе трубы. У 19 (14,6%) больных она локализовалась в истмическом отделе, где отмечались синюшного цвета утолщение данного участка, выраженное истончение и напряжение стенки трубы.
У 3 (2,3%) пациенток была диагностирована интерстициальная локализация плодовместилища – выявлено синюшно-багрового цвета патологическое утолщение одного из углов матки до 3,0 см в диаметре.
Интерстициальная локализация трубной беременности представляла определенные сложности для выполнения лапароскопической операции.
Этим больным было произведено лапароскопическое удаление трубы с иссечением угла матки с помощью биполярного инструмента и/или лигирующего и пересекающего эндоскопического инструмента с ножом LigaSure (диаметром 5 мм) с обязательным прошиванием иссеченной зоны с наложением 2–3 викриловых швов.
Морфологическую диагностику маточных труб проводили в соответствии с общепринятыми критериями [16–18]. Патологоанатомическое заключение включало указание на отдел трубы, в котором произошла имплантация, стадию развития и форму нарушения беременности.
Определение точного места эктопической имплантации плодного яйца нередко было затруднено при массивном кровоизлиянии в просвет трубы и выраженной геморрагической инфильтрации элементов трофобласта.
В таких случаях детально исследовали те участки стенки трубы, которые были наиболее плотно спаяны с прилежащим свертком крови, где была наиболее высока вероятность обнаружения ворсин хориона.
Определение стадии развития трубной беременности проводили на основании результатов клинического обследования, данных наружного осмотра удаленной трубы и ее гистологического исследования.
Выполняли гистологическое исследование всех отделов маточной трубы как в зоне имплантации плодного яйца, так и вне ее.
Кусочки ткани фиксировали нейтральным формалином, заливали в парафин, а полученные срезы окрашивали гематоксилином и эозином по Ван-Гизону и MSB-реакции на фибрин [17–19].
Результаты и обсуждение
Имплантация плодного яйца в маточной трубе приводила к значительным изменениям ее макро- и микроструктуры, которые были обусловлены инвазией ворсин хориона, формирующейся гематомой, нарушениями микроциркуляции, сопутствующими воспалительными и дистрофическими процессами.
Макроскопической оценки подлежали маточные трубы, удаленные по поводу трубной беременности. Эти изменения касались зоны имплантации плодного яйца, нарушения целостности трубы и состояния трубы вне зоны имплантации.
Макроскопически определяли локальное утолщение удаленных маточных труб, гиперемию и инъецирование серозного покрова с цианотичным оттенком над местом локализации плодного яйца, иногда определяли имбибицию тканей кровью на различном протяжении.
Макроскопические изменения маточных труб вне зоны имплантации состояли в укорочении трубы, диагностированных сращениях по серозному слою с формированием изгибов в виде «двустволок», выявлении обрывок спаек на серозном отделе.
Гистологическая картина трубной беременности характеризовалась наличием в расширенном пространстве трубы элементов плодного яйца, тканей трофобласта, сгустков крови.
В ряде случаев ворсины хориона были связаны со складками слизистой оболочки, прорастая в стенку трубы, или располагались свободно в свежей или гемолизированной крови.
В сравнении с маточной беременностью количество хориальных ворсин в эктопическом трофобласте было значительно уменьшено, причем большая часть из них была с явлениями гиалиноза. Хориальная ткань была незрелая, встречались плотные тяжи синцитио- и цитотрофобласта с лакунарными пространствами.
Гистологическое изучение серийных срезов маточной трубы вне зоны имплантации плодного яйца выявило изменения со стороны эндосальпинкса, миосальпинкса, серозного слоя и мезосальпинкса. Совокупность морфологических изменений в разных слоях трубы определяла картину хронического неспецифического продуктивного сальпингита.
Следует отметить, что морфологически наибольшие изменения в различных отделах трубы были обнаружены со стороны эндосальпинкса. Как правило, это были разной степени выраженности деформация и склероз складок эндосальпинкса, сужение просвета трубы, формирование железистых инвагинатов в мышечный слой и наличие дополнительных просветов трубы.
Для истмического отдела трубы был характерен хорошо выраженный мышечный циркулярный слой, выполняющий функцию сфинктера, и слабо выраженный слой слизистой оболочки с малочисленными уплощенными складками.
В истмическом отделе трубы определяли как укорочение, так и гипертрофию складок эндосальпинкса со склерозом стромы, сращениями между верхушками складок, формирование петлистой сети с щелевидными просветами между складками, а также атрофию складок эндосальпинкса с наличием инвагинатов желез с их кистозным расширением в миосальпинксе (рис. 1).
Рис. 1. Гистологические изменения эндосальпинкса в истмическом отделе маточной трубы: урежение, укорочение (а), сращение по верхушкам складок эндосальпинкса с формированием петлистой сети (б) и полной атрофией складок (в) с инвагинацией желез в миосальпинкс; а, б – окр. гематоксилином и эозином, в – окр. по Ван-Гизону; а – ¥100, б, в – ¥34.
Fig. 1. Histological changes of the endosalpinx in the isthmus segment of the fallopian tube: reduction, shortening (a), fusion along the tops of endosalpinx folds with forming the loop network (b) and complete atrophy of the folds (c) with invagination of the glands into the myosalpinx; a, b – hematoxylin-eosin staining, c – Van Gieson staining; a – ¥100, b, c – ¥34.
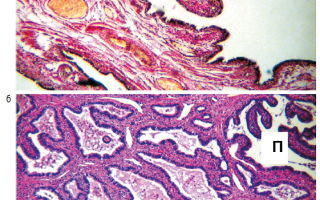
В случаях прогрессирования атрофических процессов в эндосальпинксе слизистая оболочка ампулярного отдела трубы приобретала вид коротких грубых складок со склерозом их стромы, гиалинозом стенок артериальных сосудов или подвергалась полной перестройке в виде подушкообразных утолщений с наличием разных по форме желез в толще. Это приводило к резкому сужению их просвета (рис. 2). В таких случаях деформированный щелевидный просвет трубы препятствовал прохождению оплодотворенной яйцеклетки.
Рис. 2. Морфология слизистой оболочки ампулярного отдела маточной трубы: а – крупные, грубые складки эндосальпинкса, окр. по Ван-Гизону, ¥100; б – щелевидный просвет (П) трубы с короткими складками эндосальпинкса, подушкообразным утолщением слизистой оболочки с железами в толще, окр. гематоксилином и эозином, ¥34.
Fig. 2. Morphology of the mucous membrane of the ampulla segment of the fallopian tube:
Трофобластические опухоли беременности
СПЕЦИАЛИЗИРОВАННАЯ ОНКОЛОГИЧЕСКАЯ ПОМОЩЬ www.OncoClinic.com
Трофобластические опухоли развиваются из элементов трофобласта и продуцируют хорионический гонадотропин (ХГ). Они составляют 2-6% от всех новообразований женских половых органов. Развитие их связывают либо с патологией хориального эпителия плодного яйца, либо с нарушением иммунного и гормонального статуса в материнском организме.
К факторам риска возникновения трофобластических опухолей относятся: возраст женщины после 40 лет, низкий уровень эстрогенов, а также недостаточное поступление с пищей витамина А и животных жиров. Различают пузырный занос и хориокарциному.
Пузырный занос
Пузырный занос (ПЗ) встречается у женщин относительно молодого возраста. При микроскопическом исследовании выявляются отек и ослизнение стромы ворсинок хориона с гиперплазией обоих слоев трофобласта. При полном ПЗ изменения захватывают весь хорион, при частичном — некоторую его часть. По морфологическому строению выделяют простой, пролиферирующий или деструирующий (инвазивный) ПЗ.
Клиника. Наиболее характерный клинический признак — кровянистые выделения из половых путей в сроки 10-12 нед беременности, после прерывания беременности или в послеродовом периоде.
Диагностика ПЗ может представлять большие трудности в связи с отсутствием выраженной симптоматики. Диагноз устанавливается на основе данных анамнеза, клинического, ультразвукового исследований, результатов гистологического изучения соскоба из полости матки, показателя уровня ХГ и фракций трофобластического бетта-глобулина в биологических средах организма.
Лечение заключается в незамедлительном опорожнении матки (выскабливание, пальцевая эвакуация, вакуум-аспирация, медикаментозное родовозбуждение, кесарево сечение) с последующим динамическим контролем за уровнем ХГ.
Если в течение 1-2 мес не наблюдается исчезновения ХГ, то больной показана монохимиотерапия (метотрексат или дактиномицин) и повторное углубленное обследование, чтобы исключить развитие хориокарциномы.
При инвазивном ПЗ (особенно с глубокой деструкцией миометрия) и нежелании женщины сохранить фертиль-ность, а также при профузном кровотечении показана гистерэктомия без придатков с последующей химиотерапией.
Хориокарцинома
Хориокарцинома (ХК) — злокачественная опухоль, происходящая из эпителиальных клеток ворсинок хориона. Развивается на фоне беременности или из пузырного заноса (как правило, полного). Возникает у женщин в возрасте до 50 лет.
Чаще локализуется в теле матки, реже в области патологической имплантации плодного яйца — в маточной трубе, яичнике, брюшной полости. Опухоль возникает из обоих слоев трофобласта.
Собственных стромы и сосудов не имеет, но, обладая протеолитическими свойствами, разрушает кровеносные сосуды материнского организма и разносится гематогенным путем в легкие, влагалище, печень и мозг. Характерно раннее инфицирование и некротизация.
Клиника. Проявляется кровянистыми выделениями из половых путей в любую фазу менструального цикла, прогрессирующей анемией, симптомами интоксикации, болями внизу живота. Зачастую больные предъявляют жалобы, обусловленные возникновением метастазов в легких, влагалище, головном мозге, органах желудочно-кишечного тракта.
Диагностика основывается на клинических данных, определении уровня ХГ в крови и моче, трофобластического бетта-глобулина в сыворотке крови, УЗИ органов малого таза и брюшины, ангиографии, рентгенографии легких, компьютерной и магнитно-резонансной томографии малого таза и мозга, гистологического исследования соскоба из матки (результат последнего может быть ложноотрицательным).
Классификация. Клиническая классификация злокачественной трофобластической опухоли по системе TNM и стадиям FIGO идентична. Специфичность классификаций этой опухоли состоит В учете основных прогностических факторов исхода болезни.
- TNM FIGO, категории стадии
- Т — первичная опухоль:Тх — недостаточно данных для оценки первичной опухоли,Т0 — первичная опухоль не определяется,Т1 I опухоль ограничена маткой,
- Т2 II опухоль распространяется на другие структуры: влагалище, яичник, широкую связку матки, маточную трубу в виде метастазов или прорастает их,
- M1a III метастазы в легком(их),M1b IV другие метастазы с поражением или без поражения легкого.
- Стадии FIGO подразделены на А-С соответственно факторам риска:
- А — без факторов риска;В — с одним фактором риска;
- С — с двумя факторами риска.
- Факторы риска: существуют два главных фактора риска, которые могут повлиять на исход (кроме Т и М):
1.уровень хорионического гонадотропина в моче выше 100000 IU/сут;2.признаки заболевания спустя более 6 мес от момента прерывания предшествующей беременности.
Лечение. При лечении ХК используются хирургический, комплексный, лекарственный и лучевой методы.
Эффективность хирургического метода невысока и соответствует 40% пятилетней выживаемости больных.
Показан при профузном маточном кровотечении, некротизации новообразования, склонности опухоли к перфорации, хориокарциноме плаценты, резистентности опухоли к полихимиотерапии, а также при больших размерах матки — с целью усиления эффекта от s последующего лекарственного лечения. Производится гистерэктомия (у молодых женщин — без придатков). В отдельных случаях допустима локальная резекция опухоли.
Ведущим методом лечения хориокарциномы является лекарственная терапия. Она применяется на первом этапе лечения у подавляющего большинства больных.
При неметастатической форме злокачественной трофобластической болезни и отсутствии неблагоприятных факторов прогноза обычно применяется монохимиотерапия метотрексатом или дактиномицином.
В случае неэффективности этого вида лечения, а также у всех больных метастатической формой хориокарциномы при наличии неблагоприятных факторов прогноза показана полихимиотерапия первой линии.
Используются следующие варианты лекарственного лечения:
1. Метотрексат — 30-50 мг/м2 внутримышечно еженедельно; или 0,4 мг/кг внутримышечно или внутривенно ежедневно в течение 5 дней (интервал 2 нед); или 1 мг/кг внутримышечно или внутривенно в 1, 3, 5, 7-й дни в сочетании с лейковорином — 0,1 мг/кг внутривенно во 2, 4, 6 и 8-й дни (интервал 2 нед).
2. Дактиномицин — 1,25 мг/м2 внутривенно (интервал 2 нед) или 10 мкг/кг (до 0,5 мг) внутривенно в день в течение 5 дней (интервал 2 нед).
3. Схема ЕМА/СО состоит из альтернирующих курсов:
•1-й день: этопозид — 100 мг/м2 внутривенно, дактиномицин — 0,5 мг внутривенно, метотрексат — 100 мг/м2 внутривенно бо-люсно и далее 200 мг/м2 в течение 12 ч.•2-й день: этопозид — 100 мг/м2 внутривенно, дактиномицин — 0,5 мг внутривенно, лейковорин — 15 мг внутривенно или внутрь каждые 12 ч 4 раза, начиная через 24 ч после начала введения метотрексата.
•8-й день: винкристин — 1 мг/м2 внутривенно, циклофосфан — 600 мг/м2.4. Схема MAC (интервалы между курсами 10-14 дней):•1,3, 5-й дни: метотрексат — 1 мг/кг, дактиномицин — 12 мкг/кг, циклофосфамид — 3 мг/кг внутривенно.•2-й, 4-й дни: фолиевая кислота — 0,1 мг/кг (через 24 ч после метотрексата), дактиномицин — 12 мкг/кг внутривенно, циклофосфамид — 3 мг/кг внутривенно.
•6-й, 8-й дни: фолиевая кислота — 0,1 мг/кг внутривенно.
•7-й день: метотрексат — 1 мг/кг внутримышечно.
При неэффективности схем ЕМА/СО или MAC назначают более агрессивные цисплатинсодержащие курсы полихимиотерапии второй линии.
Рекомендуется схема PVB: цисплатин — 20 мг/м2 за 4 введения в день в 1-5-й дни, винбластин — 9 мг/м2 за 4 введения в 1-й день, блеомицин — 20 мг/м2 в 1, 7 и 14-й дни либо схема Р/ЕМА: этопозид — 100 мг/м2 внутривенно в 1-й день и цисплатин — 75 мг/м2 внутривенно в 1-й день (по очереди со стандартной схемой ЕМА/СО).
Лучевой метод используется в качестве компонента химио-лучевого или комплексного лечения изолированных метастазов во влагалище, легком, параметраметральной клетчатке или головном мозге по индивидуальному плану.
У больных с хориокарциномой IV стадии уровень ХГ определяется в течение 24 мес. Клиническое обследование осуществляется всю жизнь.
Прогноз отягощен при возрасте женщины старше 39 лет, развитии болезни после родов, продолжительности периода между предшествовавшей хориокарциноме беременности и началом химиотерапии более 4 мес; уровне ХГ в моче выше 103 МЕ/л, величине матки более 7 нед беременности; размерах опухоли в матке более 3 см, наличии метастазов.
Почти все больные хориокарциномой при отсутствии неблагоприятных факторов прогноза могут быть излечены. У пациенток с наличием отягощающих прогноз факторов показатели пятилетней выживаемости составляют 60-90%.
ЗАПИСЬ НА КОНСУЛЬТАЦИЮ по телефону +7 (812) 951 — 7 — 951
Поделиться ссылкой:
Клинические протоколы. Выкидыш в ранние сроки беременности диагностика и тактика ведения
- Осмотр при помощи зеркал: источник и объем кровотечения, наличие продуктов зачатия в цервикальном канале (если есть возможность, удалить и отправить на гистологическое исследование).
- Бимануальное исследование: консистенция и длина шейки матки, состояние цервикального канала и внутреннего зева шейки матки, величина матки (в зависимости от даты последней менструации), состояние и болезненность придатков, сводов влагалища.
- Ультразвуковое сканирование
- Большинству женщин с осложнениями ранних сроков беременности требуется ультразвуковое сканирование. Трансвагинальное сканирование (ТВС), проводимое опытным специалистом, является «золотым стандартом». Если ТВС недоступно, может использоваться трансабдоминальное сканирование (ТАС), однако этот метод не так точен, как ТВС, для диагностики осложнений ранних сроков беременности.
- Плодное яйцо расположено обычно, эмбрион визуализируется, четко определяется сердечная деятельность. Наличие сердечной деятельности ассоциируется с успешным завершением данной беременности в 85-97% — в зависимости от срока гестации. Последующие назначения лекарственных препаратов и дополнительных обследований могут потребоваться в следующих ситуациях: значительное вагинальное кровотечение, субхориальная гематома, а также у пациенток с выкидышами в анамнезе или после удаления внутриматочных контрацептивов.
- 1 вариант — плодное яйцо расположено обычно, средний внутренний диаметр плодного яйца 20 мм, эмбрион не визуализируется;
- 2 вариант — плодное яйцо расположено нормально, эмбрион 7 мм, сердцебиение плода не визуализируется.
Этим пациенткам следует провести повторное сканирование через 7 дней и оценить в динамике, прогрессирует ли беременность (рост эмбриона, сердечная деятельность плода).
Ранние потери беременности:
- Трансвагинальное УЗИ должно являться стандартом обследования женщин на ранних сроках беременности. Трансабдоминальное УЗИ проводится при невозможности выполнить трансвагинальное УЗИ или для уточнения полученных данных.
Признаки ранних потерь беременности с задержкой продуктов зачатия в матке:
- при трансвагинальном исследовании средний внутренний диаметр плодного яйца > 20 мм, эмбрион не визуализируется, или при трансабдоминальном сканировании средний внутренний диаметр плодного яйца > 25 мм, эмбрион не визуализируется;
- эмбрион > 7 мм, сердцебиение отсутствует при трансвагинальном сканировании, или эмбрион > 8 мм, сердцебиение не визуализируется при трансабдоминальном УЗИ.
Если средний внутренний диаметр плодного яйца 25 мм и эмбрион не визуализируется, или если эмбрион 7 мм и нет сердцебиения, необходимо повторить УЗИ не ранее 7 дней от первоначального и оценить, есть ли динамика показателей.
NB! Вариабельность результатов измерений среднего внутреннего диаметра плодного яйца и эмбриона разными специалистами составляет 18%. В ряде случаев это может привести к ложно-положительному диагнозу неразвивающейся беременности.
В сомнительных случаях, когда получены пограничные величины среднего внутреннего диаметра плодного яйца и размеров эмбриона, необходимо провести повторное сканирование через 7-10 дней.
Диагноз неразвивающаяся беременность должен быть подтвержден двумя специалистами по функциональной диагностике, данные сохранены на бумажном и, желательно, электронном носителе.
Неполный выкидыш:
- При УЗИ в полости матки визуализируется ткань диаметром 15 мм.
Полный выкидыш:
- При УЗИ толщина эндометрия < 15 мм, а ранее были обнаружены плодное яйцо или оставшиеся продукты зачатия.
Беременность неизвестной локализации:
- Нет признаков маточной или внематочной беременности или остатков плодного яйца при наличии положительного теста на беременность или уровне ХГЧ выше 1000 МЕ/л.
- Может быть три причины того, что локализация беременности при УЗИ не выявлена: маточная беременность очень ранних сроков, полный выкидыш или ранняя внематочная беременность. Диагноз может быть установлен при последующем контрольном исследовании.
- Следует отметить, что при первом визите даже при трансвагинальном УЗИ с использованием всех критериев исследования, в 8-31% случаев невозможно установить маточная или внематочная беременность.
Уровень прогестерона
- Определение прогестерона в сыворотке крови может быть полезным дополнением к УЗИ. Уровень прогестерона в сыворотке крови ниже 25 нмоль/л является предиктором нежизнеспособности беременности. Уровень прогестерона выше 25 нмоль/л, вероятно, будет указывать на жизнеспособность беременности, а уровень выше 60 нмоль/л надежно свидетельствует о нормальном течении беременности.
- При беременности неуточненной локализации рекомендуется исследовать уровень ХГЧ в динамике, без определения прогестерона в сыворотке крови.
Узи с динамическим измерением уровня b-чхг
- Тактику лечения женщины определяют индивидуально в зависимости от клинической ситуации, предпочтений пациентки, результатов УЗИ и исследования b-чХГ.
- У 8-31% женщин при первом визите невозможно установить локализацию беременности: маточная или внематочная.
- Если поставлен диагноз полного выкидыша, следует применить все необходимые обследования, чтобы полностью исключить недиагностированную внематочную беременность.
Маточная беременность
Для потенциально жизнеспособной маточной беременности до 6-7 недель беременности, действуют следующие правила:
- Среднее время удвоения величины b-чХГ составляет 1,4-2,1 дней.
- У 85% пациенток каждые 48 часов уровень b-чХГ увеличивается на 66% и более, у 15% — на 53-66% (более 48 часов зафиксирован самый медленный прирост b-чХГ уровня на 53%).
- Маточная беременность обычно визуализируется при УЗИ, когда плодное яйцо больше или равно 3мм. Это соответствует величине b-чХГ: — 1500-2000 МЕ/л при трансвагинальном сканировании (иногда при величине b-чХГ1000 МЕ/л), или примерно 6500 МЕ/л — при трансабдоминальном сканировании, которое должно применяться только при невозможности провести трансвагинальное сканирование.
Не установлено доказанного диапазона значений для при многоплодной беременности.
Тактика ведения
Тактика ведения женщин с выкидышами в ранние сроки беременности зависит от наличия/отсутствия симптомов и того, к какой из клинических групп относится пациентка.
Выжидательная тактика
- При возникновении умеренных болей и/или скудных кровянистых выделений, наличии сомнительных данных УЗИ о жизнеспособности беременности, многие пациентки выражают желание избрать «выжидательную» позицию в надежде, что беременность все-таки закончится благополучно, или свершится выкидыш без необходимости последующего медицинского вмешательства.
- Выжидательная тактика при угрожающих и начавшихся выкидышах возможна в первом триместре беременности, когда нет клинически значимого (умеренного, обильного) маточного кровотечения, признаков инфекции, чрезмерного болевого синдрома, нарушений гемодинамики.
- Неразвивающаяся беременность — при сомнительных данных ультразвукового исследования и подозрении на неразвивающуюся беременность показано динамическое УЗИ и наблюдение за состоянием пациентки.
- В случае возникновения кровотечения из половых путей в этих случаях наблюдение должно проводиться в условиях гинекологического стационара. Необходимо проинформировать пациентку оивысокой частоте хромосомной патологии плода при спорадических ранних выкидышах, разъяснить обоснованность выжидательной тактики и нецелесообразность проведения избыточной лекарственной терапии при сомнительных данных УЗИ.
Медикаментозная терапия
- Медикаментозная терапия, направленная на пролонгирование беременности.
- При начавшемся выкидыше (схваткообразные боли, кровотечение при стабильной гемодинамике и отсутствии признаков инфекции), когда при УЗИ в полости матки обнаружено жизнеспособное плодное яйцо, показано назначение симптоматической терапии, направленной на купирование болевого синдрома и остановку кровотечения.
- Начавшийся выкидыш является показанием для госпитализации в гинекологическое отделение.
Эффективно
- Для купирования выраженных болевых ощущений (O02.1 Несостоявшийся выкидыш; O02.8 Другие уточненные аномальные продукты зачатия; O02.9 Аномальный продукт зачатия неуточненный) допустимо применение дротаверина гидрохлорида в дозе 40-80 мг (2-4 мл) внутривенно или внутримышечно.
- При выраженных кровянистых выделениях из половых путей с гемостатической целью используют транексамовую кислоту в суточной дозе 750-1500 мг. В случае обильного кровотечения возможно внутривенное капельное введение транексамовой кислоты по 500-1000 мг в сутки в течение 3 дней; при умеренных кровяных выделениях препарат применяют внутрь по 250-500 мг 3 раза в день в течение 5-7дней.
Эффективно
- Применение гестагенов при привычном выкидыше: снижается частота выкидыша по сравнению с плацебо или отсутствием лечении, не увеличивая ни частоту послеродовых кровотечений, ни вызванной беременностью гипертензии у матери.
- Схемы назначения гестагенов.
- Дидрогестерон (дюфастон)
- Угрожающий выкидыш — 40 мг однократно, затем по 10 мг через каждые 8 часов до исчезновения симптомов.
- Привычный выкидыш — 10 мг 2 раза в день до 20-й недели беременности с последующим постепенным снижением.
Микронизированный прогестерон (утрожестан)
- Привычный и угрожающий выкидыш — интравагиналъно, по 100-200 мг 2 раза в сутки до 12 недели гестации.
NB! Недопустимо одновременное назначение 2-х препаратов, имеющих однонаправленное фармакологическое действие (в данном случае — комбинировать различные гестагены).
Необоснованное назначение лекарственной терапии; одновременное назначение лекарственных средств-синонимов, аналогов или антагонистов по фармакологическому действию и т.п., связанное с риском для здоровья пациента и/или приводящее к удорожанию лечения.
Недопустимо превышать дозировку препаратов, установленную инструкцией к препарату:
- избыточные дозы препарата блокируют рецепторы, т.е. превышение доз гестагенов нарушает чувствительность рецепторов прогестерона и вместо сохранения беременности может спровоцировать выкидыш.
- Согласно инструкциям, показаниями к назначению гестагенных препаратов в первом триместре беременности являются: профилактика привычного и угрожающего аборта вследствие недостаточности прогестерона.
- Эффективность назначения гестагенов с лечебной целью при угрожающем и начавшемся спорадическом спонтанном выкидыше в настоящее время убедительно не доказана.
- Однако в систематизированном обзоре 2012 года показано, что при использовании дидрогестерона риск самопроизвольного аборта снижается на 47%.
- Неэффективно.
- Назначение постельного режима при начавшемся выкидыше не повышает частоту благоприятных исходов беременности (уровень доказательности В).
- В настоящее время отсутствуют убедительные доказательства эффективности и обоснованности применения препаратов магния при выкидыше в ранние сроки беременности.
- При неэффективности проводимой медикаментозной терапии и/или отрицательной динамике по данным УЗИ следует пересмотреть тактику ведения, обсудив ее с пациенткой.
- NB! Ультразвуковые признаки, свидетельствующие о неблагоприятном исходе маточной беременности:
- отсутствие сердцебиения эмбриона с копчиково-теменным размером более 7 мм;
- отсутствие эмбриона при размерах плодного яйца (измеренных в трех ортогональных плоскостях) более 25 мм при трансвагинальном сканировании.
Дополнительные признаки
- аномальный желточный мешок, который может быть больше гестационного срока, неправильной формы, смещен к периферии или кальцифицирован;
- частота сердечных сокращений эмбриона менее 100 в минуту при гестационном сроке 5-7 нед. беременности;
- большие размеры ретрохориальной гематомы — более 25% поверхности плодного яйца.
Профилактика спонтанного выкидыша
Методов специфической профилактики спорадического выкидыша не существует. Пациентки должны быть проинформированы о необходимости своевременного обращения к врачу во время беременности при появлении болей внизу живота и кровянистых выделений из половых путей.
Неэффективно назначать:
- постельный режим
- половой покой
- ХГЧ
- средства, релаксирующие матку
- эстрогены
- прогестерон (перорально, интравагинально, внутримышечно) — за исключением пациенток с привычным невынашиванием
- моно- и поливитамины
Эффективно:
- профилактическое введение препаратов прогестерона (перорально, внутримышечно, вагинально) женщинам с привычным выкидышем в первом триместре.
- Для профилактики дефектов нервной трубки и других пороков развития, которые частично приводят к ранним самопроизвольным выкидышам, рекомендован прием фолиевой кислоты за два-три менструальных цикла до зачатия и в первые 12 недель беременности в суточной дозе 400 мкг (0,4 мг).
- Если в анамнезе у женщины в течение предыдущих беременностей отмечены дефекты нервной трубки плода, профилактическая доза фолиевой кислоты должна быть увеличена до терапевтической 3-5 мг/сут.
- Профилактика имплантационных потерь после применения ВРТ.
Эффективно: применение прогестерона для поддержки лютеиновой фазы после применения ВРТ, так как позволяет повысить частоту прогрессирования беременности и живорождения. Способ введения прогестерона не имеет значения . При назначении гестагенной поддержки после ВРТ следует следовать инструкциям к препаратам и соблюдать общие принципы назначения лекарственных средств.
Неэффективно: использование эстрогенов и ХГЧ для поддержки лютеиновой фазы после применения ВРТ не улучшает исходы, при этом использование ХГЧ ассоциировано с увеличением частоты синдрома гиперстимуляции яичников.
Прогноз
Прогноз, как правило, благоприятный. После одного самопроизвольного выкидыша риск потери следующей беременности возрастает незначительно и достигает 18-20% по сравнению с 15% при отсутствии выкидышей в анамнезе.
- При наличии двух последовательных самопроизвольных прерываний беременности рекомендовано обследование до наступления желательной беременности для выявления причин невынашивания у данной супружеской пары.
- Психологические аспекты невынашивания беременности на ранних сроках.
- Врачи всех специальностей должны знать психологические последствия, связанные с выкидышем, и должны оказать психологическую поддержку и последующее наблюдение, а также обеспечить доступ к профессиональному психологическому консультированию (уровень доказательности рекомендаций В).
Ранний выкидыш отрицательно воздействует на психическое состояние определенной части женщин, их супругов и других членов семьи (уровень доказательности III).
Для некоторых женщин психологическая травма оказывается достаточно серьезной и продолжительной, даже если выкидыш происходит в самом начале беременности.
И этот факт не может быть не принят во внимание специалистами, оказывающими медицинскую помощь таким пациенткам.
Женщинам, перенесшим выкидыш, должна быть предоставлена возможность для получения дальнейшей помощи. В оказание помощи могут быть вовлечены не только врачи, занимавшиеся пациенткой на этапе выкидыша, но и работники службы первичной медицинской помощи (врачи общей практики, медсестры, акушерки, патронажный персонал), службы психологической поддержки и консультирования.
Планы давнейшего ведения должны быть ясно изложены пациентке в рекомендациях при выписке